On sait que l'atome est composé d'un noyau et d'électrons qui tournent autour de celui-ci. Il arrive que des électrons passent d'une couche à une autre, suite à une réception ou une émission d'un photon par exemple. Mais le vide qui sépare les différentes couches et le noyau, comment l'appelle-t-on ? Et comment définit-on la "limite", le "diamètre" d'un atome ?
-
A l'intérieur de l'atome
- La physique quantique est l'appellation générale d'un ensemble de théories physiques qui s'opposent à celle de physique classique, cette dernière ayant échoué dans la description de l'infiniment petit (atomes, particules) et dans celle de certaines propriétés du rayonnement électromagnétique. La physique quantique comprend : l'ancienne théorie des quanta, les postulats de la mécanique quantique, la mécanique quantique non relativiste, la physique des particules, la physique de la matière condensée, la physique statistique quantique, la chimie quantique, les théories candidates à une description de la gravité quantique.
- Accueil
- Théories cosmologiques Physique Quantique et théories quantiques « Vous êtes ici
je voudrai aporter une précision les électrons qui passe d un atome a l autre se nome des {élèctrons libres] un atome et constitué de neutron et de proton d ou gravite autour les électron a trés grande vitesse .
En attendant que Bongo vienne éclairer nos lanternes....
Cette vision de l'électron qui tourne autour du noyau façon planète autour du Soleil, bref de la mécanique newtonienne, n'est pas celle qui prévaut. On est ici à l'échelle atomique, voire subatomique où règne la mécanique quantique.
Les électrons ont des "probabilités" de présence et de niveau d'énergie (état). Bref il n'y a pas de "couche" comme tu les décrit, ni de vide entre ces couches.
Qui plus ait, vu la taille des électrons, neutrons et protons, ce qu'il y a de vide c'est ... tout !
Même au sein des atomes il y a plus de vide que de matière.
Sinon je ne sais pas si le "vide" dont tu parles à un nom.
Cette vision de l'électron qui tourne autour du noyau façon planète autour du Soleil, bref de la mécanique newtonienne, n'est pas celle qui prévaut. On est ici à l'échelle atomique, voire subatomique où règne la mécanique quantique.
Les électrons ont des "probabilités" de présence et de niveau d'énergie (état). Bref il n'y a pas de "couche" comme tu les décrit, ni de vide entre ces couches.
Qui plus ait, vu la taille des électrons, neutrons et protons, ce qu'il y a de vide c'est ... tout !
Même au sein des atomes il y a plus de vide que de matière.
Sinon je ne sais pas si le "vide" dont tu parles à un nom.
Oui, je sais bien que la vision de l'électron qui orbite autour de l'atome n'est pas réaliste, mais il faut bien se donner une "représentation". C'est vrai qu'il y a du vide partout partout, mais est-ce l'absence de matière, y a-t-il de l'énergie ?
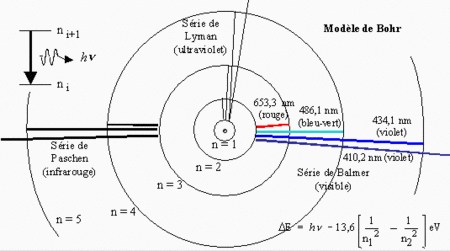
Effectivement, comme le dit Gbs, le modèle atomique de Bohr est une très grosse approximation de la réalité qui date de 1913. Ce modèle a juste le mérite d'expliquer les séries de Balmer, Lyman, Paschen etc... en supposant la quantification du moment cinétique. Par contre... l'atome de Bohr n'arrive pas à expliquer les autres atomes.
En 1925, c'est le modèle de Schrödinger. Il est un peu plus abstrait. Il repose sur des orbitales atomiques. Ce sont les orbitales 1s, 2s, 2p, 3s, 3p, 3d etc...
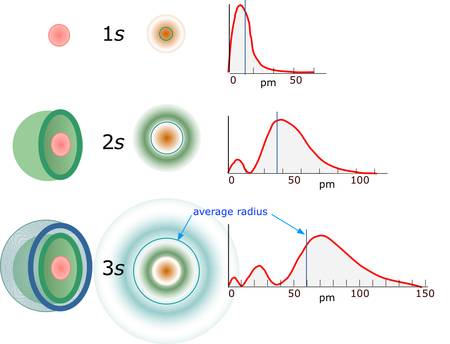
Comme tu peux le voir par exemple pour la fonction d'onde 1s, donc c'est elle qui décrit la probabilité de présence de l'électron autour du proton dans l'état fondamental (de plus basse énergie).
On voit que la probabilité de présence au voisinage du proton est pratiquement nulle, puis augmente jusqu'à une certaine distance, puis diminue à nouveau. L'amplitude est pilotée par une fonction du genre r * exp(-r/a0).
Donc tu as une probabilité non nulle de trouver l'électron très loin du noyau.
En pratique on considère qu'à quelques multiples de a0, la probabilité est très très faible.
Pour l'orbitale suivante la 2s, tu vois que la probabilité de présence de l'électron ne diminue que bien plus loin du noyau. Mais elle s'annule 2 fois (une fois au voisinage du noyau, et une autre fois un peu plus loin).
etc...
Donc comme tu vois, quand l'électron passe d'une couche à une autre... et bien... ce n'est pas aussi simple que des sauts d'orbite.

En 1925, c'est le modèle de Schrödinger. Il est un peu plus abstrait. Il repose sur des orbitales atomiques. Ce sont les orbitales 1s, 2s, 2p, 3s, 3p, 3d etc...

Comme tu peux le voir par exemple pour la fonction d'onde 1s, donc c'est elle qui décrit la probabilité de présence de l'électron autour du proton dans l'état fondamental (de plus basse énergie).
On voit que la probabilité de présence au voisinage du proton est pratiquement nulle, puis augmente jusqu'à une certaine distance, puis diminue à nouveau. L'amplitude est pilotée par une fonction du genre r * exp(-r/a0).
Donc tu as une probabilité non nulle de trouver l'électron très loin du noyau.
En pratique on considère qu'à quelques multiples de a0, la probabilité est très très faible.
Pour l'orbitale suivante la 2s, tu vois que la probabilité de présence de l'électron ne diminue que bien plus loin du noyau. Mais elle s'annule 2 fois (une fois au voisinage du noyau, et une autre fois un peu plus loin).
etc...
Donc comme tu vois, quand l'électron passe d'une couche à une autre... et bien... ce n'est pas aussi simple que des sauts d'orbite.
Et qu'est-ce que sont les séries de Balmer, Lyman et Paschen ?
En effet, je vois ça ! Je n'avais jamais vu ces schémas de fonction d'onde, c'est intéressant.
Donc comme tu vois, quand l'électron passe d'une couche à une autre... et bien... ce n'est pas aussi simple que des sauts d'orbite.
En effet, je vois ça ! Je n'avais jamais vu ces schémas de fonction d'onde, c'est intéressant.

